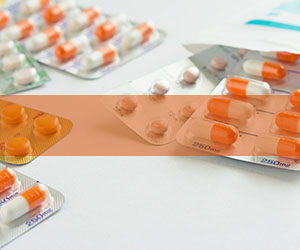
中国のsiRNA企業ARGOは患者に希望をもたらす
– 中国のspecialty biopharmaに見る、かつてない選択と集中、スピード、パワー
編集長コメント (2024年2月12日発行、第67号に寄せて)
今回の医薬研発達人第67号では、第65号(2024年1月15日発行)「中国発抗PD-1モノクローナル抗体は如何にして初のFDA承認を得られたのか?」、第66号(2024年1月29日発行)「2023年、大手多国籍製薬企業が中国企業から導入した新薬」に引き続き、3号連続で、近年成長著しい中国製薬企業の世界進出について取り上げる。
第65号では、昨年10月に米国承認を成し遂げた抗PD-1抗体薬toripalimabに焦点を当てたが、今号では将来が有望視されている中国発の核酸医薬、短鎖干渉RNA; small interfering RNA, siRNAに着眼する。
siRNA医薬は、体外で化学合成した低分子2本鎖のsiRNAを細胞内に送り込んで標的mRNAの分解を誘導することにより、そのmRNAによるたんぱく質合成を妨げるというRNA干渉 (RNA interference, RNAi) システムを応用した新規モダリティで、2002年に米国で設立されたAlnylam Pharmaceuticals社が世界のパイオニアかつリーダーである。同社品は、2018年8月のONPATTRO (patisiran) の米国承認を皮切りに、米国で既に4製品が承認されていて、それら製品は順次、欧州や日本を含め世界展開されており、また臨床開発中のパイプラインは20品目にも上る。
siRNA医薬は、異常なたんぱく質が原因となって発症する疾患の治療に広く使えるため、ターゲットとなる疾患は非常に多く、遺伝性疾患や希少疾患はじめ、循環器領域やCNS領域や生活習慣病まで、実に多岐に及ぶ。
また、siRNA医薬は、疾患の原因となるたんぱく質と標的mRNAを見定めた上で開発するので、臨床開発ステージでの失敗確率が低い。
そのような理由もあって、2020年頃から、Global giant pharmasが次々とsiRNA医薬を持つ米国等の企業をM&Aしたり、ライセンス・アライアンス契約を締結したりするなど、ここ数年siRNA医薬には世界から熱い視線が注がれている。
さて、今号で特集した上海に本社を置く舶望製薬 (Argo Biopharma) のホームページ (https://www.argobiopharma.com/) を覗くと、企業のMissionにもVisionにもRNA技術・RNA療法が謳われているなど、今号の本文中に詳細に記載したとおり、siRNA医薬に特化した製薬企業であることが見て取れる。
トップページに現れる表などによれば、同社は、2021年設立でまだ3年にも満たず、社員数も60余名程度なのに、これまでに100 mil USDを超える資金調達を受け、23件の特許協力条約 (Patent Cooperation Treaty, PCT) に基づく国際特許出願を行い、30品目以上の研究開発パイプラインを有し、うち5品目では既に臨床開発入りしている。
なお、同社の臨床開発は、オーストラリアや中国を中心に行われ、CDEの臨床試験情報登録プラットフォームで検索すると、いずれも杭州舶临医药科技を申請人、上海市徐汇区中心医院を主要研究者兼参加施設として、CTR20232382 (BW-00112、脂質異常症)、CTR20233376 (BW-20805、遺伝性血管性浮腫)、CTR20233485 (BW-00163、高血圧症) の3本のphase 1二重盲検国内試験が実施中である。
| 2024年2月8日(木)に厚労省で開催された「第8回創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会」におけるボストンコンサルティンググループ柳本岳史構成員からの提出資料には、次のような見出しがある。 ・新規モダリティに着目したとき、ドラッグロスは拡大傾向であり、現時点で35%、将来的には~75%が日本では使えなくなる可能性 ・具体的なモダリティを見たとき、将来的には再生細胞医療や遺伝子治療薬、核酸医薬をはじめとして多くの製品が“ドラッグロス“に陥る懸念 柳本氏の分析によれば、再生細胞医療、遺伝子治療、核酸医薬においては、日本で、既にドラッグロスが顕在化しており、今後さらに拡大する見込みとのことである。 https://www.mhlw.go.jp/stf/newpage_37787.html |
中国の核酸医薬に関しても、これまでのところは、中国での承認薬は輸入品に頼っていて、ドラッグラグも生じているが、舶望製薬 (Argo Biopharma) はじめ、いくつもの中国企業が、米欧の外国企業と提携するなどして、現在、中国内外でsiRNA医薬の研究開発を進めており、中には、今号の本文中にも記載したとおり、中国発の核酸医薬がGlobal giant pharmaに世界導出されるケースまで既に存在している。
あくまでも、現時点での筆者の個人的な感触に過ぎないが、中国の将来の核酸医薬におけるドラッグロスは、日本ほど深刻ではないかも、と感じる。
一般論として、日本の創薬ベンチャーは、パイプライン、資金、人材のいずれもが潤沢でなく、またそれらの供給源が国内に限定され、臨床開発も国内試験が主流であり、それらは密接に相互に関連していると聞く。従って、Initial Public Offering, IPOに際しては国内の東証を目指すし、自社単独でProof of Concept, POCを取るのは容易でなく、世界的な大型導出にはほとんど結び付かない。
一方、米国の創薬ベンチャーは、パイプライン、資金調達、専門的な人材が、いずれも豊富かつ国際的であり、当然、臨床開発はMulti-Regional Clinical Trial, MRCTであり、米国NASDAQでの上場を目指し、自社単独でPOCを取り、中には自社でNDA/BLA承認まで成し遂げ、Global giant pharmasへの大型導出やM&Aを出口戦略としている。
そして、中国の新興biopharmaは、日米の中間というよりは米国にだいぶ近いと感じる。資金調達は中国国内がメインで、IPOは通常、香港市場や上海市場であるが、パイプライン(の種)や人材の多くは米国帰りで、自社単独でPOC以降の後期phase試験も中国国内やMRCTで行い、自社で中国承認を成し遂げるとともに、Global giant pharmasへの世界的な導出を目指している。
近年の中国の新興biopharmaのビジネスモデルには、日本再浮上のヒントが必ずある。
高野 哲臣(t2T Healthcare株式会社代表取締役社長)
続きは、以下のリンク先をご参照ください。
https://mp.weixin.qq.com/s/AiKX6ZXa7iWd6rwFirNQ4Q